免疫组化的未来发展方向随着技术的进步,免疫组化在未来将朝着更高灵敏度、更高通量和更自动化的方向发展。高灵敏度技术(如信号放大系统)将能够检测更低丰度的目标蛋白。高通量技术(如组织芯片)将能够同时检测多个样本或多个目标蛋白。自动化技术(如自动染色仪)将能够提高实验的标准化和重复性。此外,免疫组化还将与其他技术(如质谱分析、单细胞测序)结合,提供更***的蛋白质表达和功能信息。这些技术的发展将推动免疫组化在生物医学研究和临床诊断中的应用。本回答由 AI 生成,只供参考,不构成任何专业建做好免疫组化,你需要了解这些!黑龙江组织免疫组化要多久
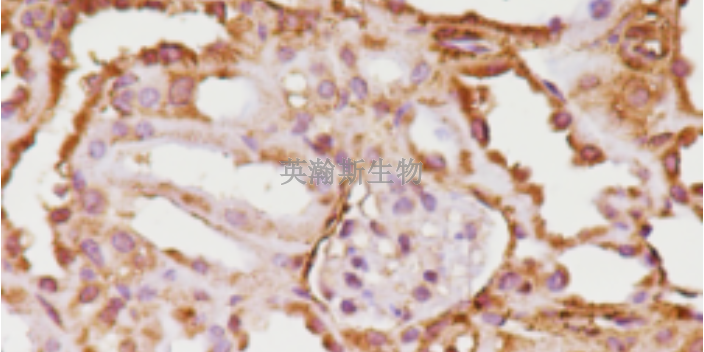
确定cancer分期,免疫组化技术应用于临床可以进行处理哦,英瀚斯生物为您处理。cancer分期是判断预后的一个指标,与是否浸润、有无淋巴管或血管侵袭密切相关,而通过免疫组化方法可以判断cancer是否浸润、有无淋巴管或血管侵袭。层黏连蛋白和Ⅳ型胶原的单克隆抗体可以清楚的显示基膜的主要成分,用于区分原位*和浸润*,一旦上皮性*突破基膜为浸润,未突破基膜为原位;显示血管和淋巴管内皮细胞的标记物第八因子相关蛋白、D2-40等则可清楚显示cancer对血管或淋巴管的浸润。因此对许多cancer的良恶性鉴别及有无血管或淋巴管浸润,免疫组化结果作为主要的鉴别依据。黑龙江组织免疫组化要多久免疫组化样本如何处理?
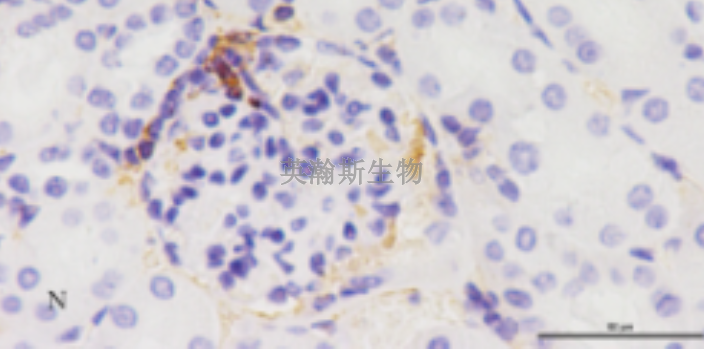
免疫组化技术应用于临床cancer良恶性的判断,英瀚斯生物为您介绍。对于反应性增生还是cancer性增生,可用免疫球蛋白(Ig)的轻链抗体检测B淋巴细胞增生的单克隆或多克隆性来区别。在滤泡反应性增生时,滤泡反应中心的细胞不表达细胞凋亡蛋白(bcl-2),bcl-2阴性;而在滤泡性淋巴瘤中,由于90%以上cancer性滤泡细胞有bcl-2的高表达,bcl-2阳性。而增殖细胞核抗原(PCNA),周期素(Cycling),核抗原(Ki-67)通过对cancer细胞增生的程度作出评价,从而提示增生细胞的良恶性。
免疫组化的实验步骤
免疫组化的实验步骤通常包括组织固定、切片、抗原修复、封闭、一抗孵育、二抗孵育、显色和复染等。首先,组织样本需要经过固定(如福尔马林固定)以保持其形态结构。然后,将固定后的组织包埋在石蜡中并切成薄片。抗原修复是为了暴露被固定过程掩盖的抗原表位,常用的方法有热修复和酶消化。封闭步骤是为了减少非特异性结合,通常使用血清或BSA。一抗孵育是关键步骤,一抗与目标蛋白特异性结合。二抗孵育则是通过二抗与一抗结合,并连接显色系统。,通过显色和复染使目标蛋白可视化。 免疫组化可以看什么?

免疫组化有哪几种分类 ?
1)按标记物质的种类,如荧光染料、放射性同位素、酶(主要有辣根过氧化物酶和碱性磷酸酶)、铁蛋白、胶体金等,可分为免疫荧光法、放射免疫法、免疫酶标法和免疫金银法等。
2)按染色步骤可分为直接法(又称一步法)和间接法(二步、三步或多步法)。与直接法相比,间接法的灵敏度提高了许多。
英瀚斯生物病理染色效果好,效率高。
3)按结合方式可分为抗原-抗体结合,如过氧化物酶-抗过氧化物酶(***)法;亲和连接,如卵白素-生物素-过氧化物酶复合物(ABC)法、链霉菌抗生物素蛋白-过氧化物酶连结(SP)法等,其中SP法是比较常用的方法;聚合物链接,如即用型二步法,此方法尤其适合于内源性生物素含量高的组织抗原检测。 英瀚斯生物实验外包,多种病理染色熟练掌握,可做免疫组化!黑龙江组织免疫组化要多久
免疫组化失败的原因?黑龙江组织免疫组化要多久
免疫组化实验所用的抗体
免疫组化实验中常用的抗体为单克隆抗体和多克隆抗体。单克隆抗体是一个B淋巴细胞克隆分泌的抗体,应用细胞融合杂交瘤技术免疫动物制备。多克隆抗体是将纯化后的抗原直接免疫动物后,从动物血中所获得的免疫血清,是多个B淋巴细胞克隆所产生的抗体混合物。
免疫组化就找英瀚斯,高效率,高质量。
免疫组化常用的染色方法
根据标记物的不同分为免疫荧光法,免疫酶标法,亲和组织化学法,后者是以一种物质对某种组织成分具有高度亲合力为基础的检测方法。这种方法敏感性更高,有利于微量抗原(抗体)在细胞或亚细胞水平的定位,其中生物素—抗生物素染色法常用。 黑龙江组织免疫组化要多久