危机应对与应急递交机制 在公共卫生紧急事件(如COVID-19)中,EMA允许简化eCTD序列,优先审评关键模块并暂缓非数据。申请人可通过快速通道(Fast Track)提交疫苗或药物的eCTD资料,审评周期可压缩至6个月。此类申请需附风险评估报告,并承诺后续补交完整数据。 数据安全与长期存档 欧盟要求eCTD资料存档期限至少为药品上市后30年,EMA采用分布式存储和区块链技术确保数据不可篡改。申请人需定期备份本地副本,并使用符合GDPR要求的加密传输协议(如AS2)递交。历史数据的迁移和格式转换(如NeeS转eCTD)需遵循特定技术规范。 环保效益与可持续发展 eCTD取代纸质递交后,欧盟每年减少约500吨纸张消耗,审评流程的数字化降低碳足迹约30%。虚拟审评会议和电子签名进一步减少了差旅需求,契合欧盟2050碳中和目标。未来,eCTD4.0将通过数据压缩技术进一步降低服务器能耗。加拿大eCTD验证标准相关技术支持。美国eCTD报价
澳大利亚的药品电子通用技术文档(eCTD)注册申报体系是澳大利亚y药品商品管理局(TGA)推动药品审评现代化的重要举措。eCTD作为国际通行的电子化注册申报标准,通过结构化数据格式(如XML)整合了药品质量、安全性和有效性的技术文档,实现了从传统纸质递交向数字化流程的转型。根据TGA要求,eCTD需遵循通用技术文档(CTD)框架,分为五个模块:模块1包含澳洲特定的行政信息(如产品说明书草案和GMP证明);模块2为质量、非临床及临床研究的综述与总结;模块3至模块5则分别涵盖药学、非临床和临床的详细数据。澳大利亚自2024年起加速推进eCTD实施,要求创新药注册申报优先采用该格式,以提升审评效率并支持全球同步申报。 申报流程上,企业需通过TGA指定的电子提交门户(如eSubmission Gateway)上传eCTD序列,并在受理后5个工作日内同步提交纸质版模块1-5资料。浦东新区CDE eCTD供应商加拿大DMF注册申报关技术支持。

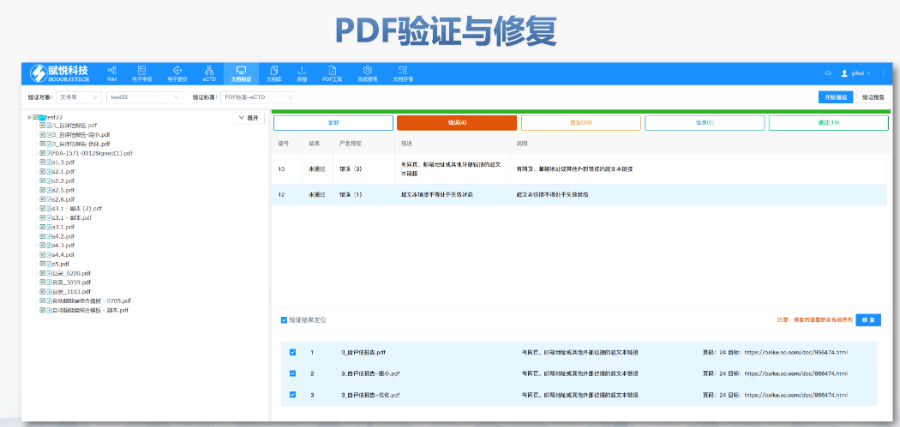
eCTD提交流程与ESG系统:FDA要求通过电子提交网关(ESG)传输eCTD文件,单个文件大小限制为10GB,超限需拆分或通过物理介质(如光盘)递交。提交前需预分配申请号(如NDA编号),并通过ESG测试账户验证技术合规性。序列号命名规则为4位数字(如0001),申请需从“原申请”序列开始,补充资料按递增顺序编号。企业可自愿提交预审样本(Pre-Submission),FDA将反馈文档结构、元数据等合规性问题。验证标准与常见错误类型:FDA验证标准分为高(High)、中(Medium)、低(Low)三级,高风险错误(如无效XML或缺失关键表格)必须修复,否则直接拒收。常见问题包括:重复序列号(错误1034)、文件路径超长(警告2015)、PDF加密或非标字体(错误4001)。2023年统计显示,30%的提交因模块1格式错误被退回,凸显行政信息合规的重要性。验证工具如LORENZ eValidator被FDA官方采用,可自动检测200+项技术指标。
生命周期管理与变更递交 eCTD支持全生命周期管理,申请人需通过序列更(Sequence)反映药品变更信息。例如CEP证书的更需提交“变更说明表”,对比已批准和拟修改内容,并附修订版技术文档。重大变更(如生产工艺调整)可能触发GMP现场检查,EDQM将根据风险评估决定是否启动核查。 电子签名与法律效力 欧盟接受符合《电子签名法》的数字签名,手写签名的扫描件需嵌入PDF并加密保护。模块1的申请表和承诺书必须包含有效签名,且XML文件需通过MD5校验确保完整性。若使用第三方签署工具,需提前向监管机构报备并获取技术认可。 中小企业支持与资源获取 EMA和EDQM为中小企业提供eCTD实施指南、验证工具及培训研讨会。例如,EDQM官网发布CEP递交模板和案例库,EMA则定期更Q&A文档以解答常见问题。此外,欧盟设立专项基金,资助中小企业完成eCTD转换和系统部署。加拿大eCTD申报软件相关技术支持。

内容与格式检查Word预处理:需检查拼写、缩略语、单位格式(如),设置多级列表自动编号(如),统一字体(宋体/TimesNewRoman)和段落格式。重复内容处理:相同剂型不同规格可共用模块3,但需区分包装系统(如、)。外文资料:中文在前、原文在后,参考文献需中英文对照并建立跨网页链接。使用符合ICH标准的eCTD编辑器自动生成XML骨架和MD5校验值,拖拽PDF文件构建结构树。序列管理:序列号从0000开始递增,每次提交需更新序列,生命周期状态(New/Replace/Delete)需在XML中明确标注。验证与递交:确保无验证错误(如书签缺失、超链接断链),通过ESG等电子通道传输,光盘封面需包含申请号和序列号。全生命周期管理版本:通过软件实现网页签入/签出、审批流程,支持历史版本追溯。变更管理:增补(Append)和替换(Replace)需关联原始序列,删除(Delete)需彻底移除无效文件。 瑞士IND注册申报相关技术支持。安徽eCTD哪个品牌好
欧盟CESP提交通道相关技术支持。美国eCTD报价
eCTD验证标准的严格性与分类:欧盟对eCTD的验证要求分为“错误”“警告”和“提示信息”三级,其中“错误”项直接导致申报被拒。验证项目涵盖六大类共149条,包括文件命名规范(如路径长度限制)、PDF可读性(禁止密码保护)、XML骨架文件完整性等。例如,文件扩展名必须符合规范(如.xpt用于临床数据集),而文件夹层级需避免空目录或混合存放文件。相较于中国《电子申报验证标准》的简化版(54条),欧盟的验证体系更为复杂,体现了其高标准的技术监管。美国eCTD报价
赋悦科技由生物制药行业老师、医药信息化工程师以及具有丰富经验的互联网软件工程师组成,为医药行业用户提供专业的药品注册申报工具软件与服务,如eCTD系统、电子申报系统,注册管理系统,PDF工具箱等。 赋悦科技有多名药品注册顾问老师,国内重点医药院校教授,为生命科学企业提供药品、生物制品、医疗器械、化工品等注册咨询与外包服务。擅长领域包括国际药品注册,进口药品注册,中国药品注册等,成功向中国、美国、欧盟、加拿大、澳大利亚、巴西、印度、日本等10多个国家提交注册申报材料,包括DMF,CEP,ASMF,ANDA,IND等。