经济影响与成本效益 尽管初期投入较高(平均每企业需50万欧元),但eCTD可减少30%的审评延迟成本,长期效益。仿制药企业通过eCTD复用原研数据,节省80%的申报准备时间。欧盟预算拨款2亿欧元资助中小企业完成数字化转型。 伦理审查与数据隐私 eCTD中的患者数据需匿名化处理,符合《通用数据保护条例》(GDPR)要求。临床试验模块(模块5)的提交需附带伦理委员会批准文件,且区域版本需体现各国伦理审查差异。AI辅助匿名化工具在保护隐私的同时提升数据处理效率。 技术融合与跨领域应用 eCTD格式扩展至医疗器械和保健品领域,欧盟试点eCTD-MDR项目整合ISO标准。基因产品的eCTD需附加生物安全数据库,并与欧盟基因库实时同步。未来,eCTD或与电子健康档案(EHR)系统对接,支持个性化用药。 持续改进与行业反馈机制 EMA每年发布eCTD实施报告,分析常见错误并更指南。行业联盟(如EFPIA)通过定期研讨会向监管机构反馈技术痛点,推动标准优化。开放式API接口的推广将促进eCTD工具链的互操作性,降低技术锁定风险。澳大利亚eCTD注册外包相关技术支持。苏州中国eCTD供应商
ANDA一般不需要提供临床前(动物)和临床(人体)数据来证明其安全性和有效性(即免毒理和临床),作为替代,申请人必须合理证明其产品与原研药相比是生物等效的。 按照《联邦食品、药品和化妆品法》第 505(j)章要求,拟向FDA递交申请ANDA的药品需符合以下条件: 仿制药必须依照FDA《经过医疗等同性评价批准的药品》(俗称"橙皮书")上所列,由FDA选定的RLD/RS进行对照仿制; 活性成份、剂型、规格、给药途径、适应症,要与RLD相同; 仿制药必须证明与RLD在生物效果上等同,即具有生物等效性; 必须按照美国联邦管理法21 CFR遵行药品生产管理规范控制生产过程; 无论中国还是美国,要求仿制药的质量必须等同或者是高于参比制剂的,这是获批的基本要点; 注意:如果原研药未被列为RLD,申请人可以提出公民,向FDA申请。上海NDAeCTD报价欧盟NDA注册申报相关技术支持。
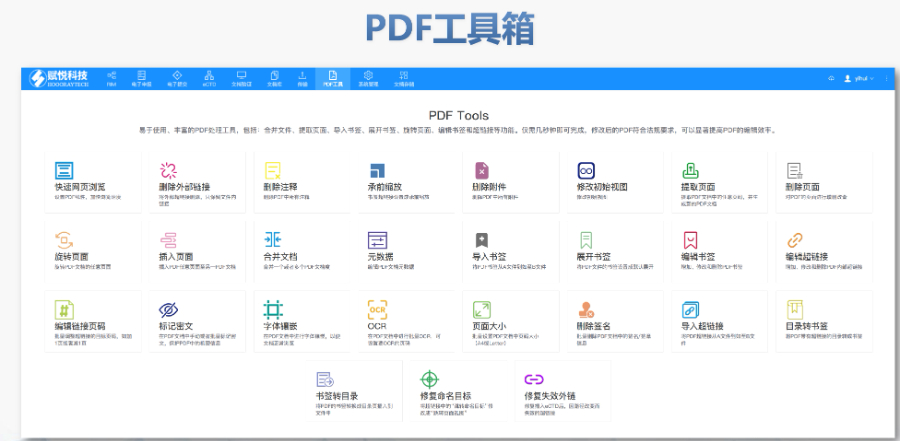
美国eCTD的强制实施时间与范围:美国自2017年5月5日起要求药申请(NDA)、仿制药申请(ANDA)和生物制品许可申请(BLA)必须通过eCTD格式提交,2018年5月5日进一步扩展至临床试验申请(IND)和药品主文件(DMF)。FDA通过《联邦食品、药品和化妆品法案》第745A条明确电子提交的强制性,豁免非商业化IND和部分DMF类型(如Ⅲ类)。2023年数据显示,FDA接收的eCTD申请占比已达92%,标志着电子化审评体系的成熟。企业若未按规范提交(如缺少文件或重复序列号),将直接被拒收。
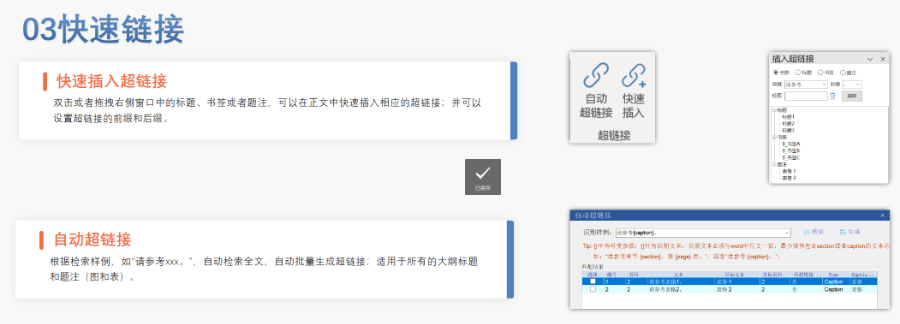
eCTD的技术架构与模块要求:美国eCTD基于XML技术,严格遵循ICH M4框架,分为5个模块:模块1(地区行政信息)、模块2(技术总结)、模块3-5(质量、非临床与临床数据)。其中,模块1需包含FDA特定的文件,涵盖申请编号、联系人和DMF授权书等行政信息。模块2-5需与ICH CTD全球统一标准一致,但FDA对文件颗粒度要求更细,例如非临床研究报告需拆分并标记Study ID。PDF文件需符合FDA v4.1格式规范,包括字体嵌入、书签层级和超链接功能。瑞士eCTD注册申报相关技术支持。
仿制药作为提高药物可及性与可负担性的一类药物,2012年以前,注册审评是不收取任何费用的,但当时仿制药申请积压严重,从申报到获批需要3~5年的时间。 美国国会于2012年颁布了仿制药使用者费用修正案(Generic Drug User Fee Amendments, GDUFA),该法律要求制药行业支付一定的用户费用,以补充仿制药申请的审评以及现场检查的费用,减少仿制药申请积压,缩短审评时间,增加基于风险的现场检查等,其目的是加快公众获得安全有效的仿制药,并降低行业成本。 GDUFA必须每五年重授权一次,于2017年更(GDUFA II),于2022年更(GDUFA III); 目前收费种类分为以下四种:ANDA审评费、DMF审评费,在审评时一次性缴纳;项目费(Program fee)、设施费(Facility fee),是上市后每年缴纳一次。欧盟eCTD验证标准相关技术支持。徐汇区赋悦科技eCTD哪个品牌好
瑞士eCTD验证标准相关技术支持。苏州中国eCTD供应商
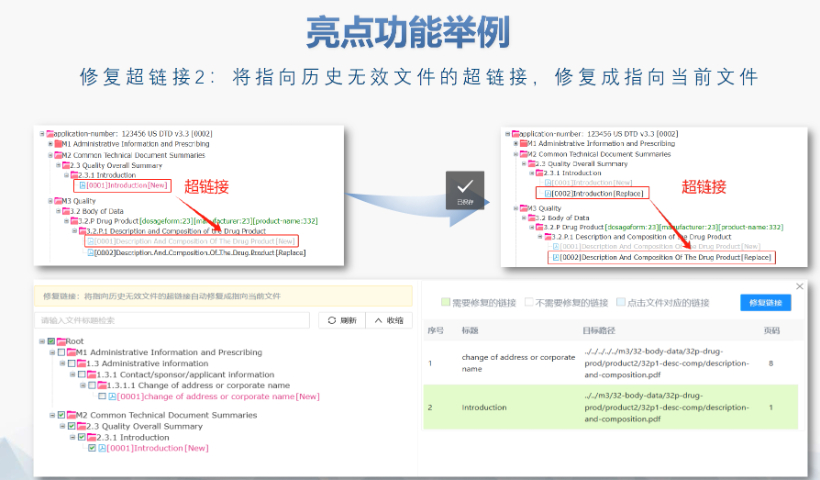
文件生命周期管理:eCTD支持文件替换(Replace)、删除(Delete)等操作,而非增文件。例如,更临床研究方案时需用Replace操作覆盖旧版本。基线提交(Baseline Submission)可用于补充历史纸质资料,但需在封面函中声明无内容变更。 临床数据与研究标签文件(STF):模块4和5中的研究数据需通过STF(Study Tagging Files)引用,确保数据与文档关联。FDA要求数据集(如SAS XPORT格式)能置于模块3-5,且单个文件超过4GB需拆分。2022年统计显示,58%的ANDA因研究数据技术拒绝标准(TRC)错误被拒。 电子签名与表格要求:FDA表格(如356h、1571)需使用数字签名,PDF文件禁止加密或设置编辑限制。电子签名需符合21 CFR Part 11规范,确保身份验证、不可否认性和数据完整性。 外包服务与系统解决方案:赋悦科技累计提交超2000份eCTD申请,外包可降低40%人工错误率。苏州中国eCTD供应商