采用气管内注射博莱霉素(Bleomycin,BLM)的方法,比较观察两个品系小鼠肺纤维化程度,确定适用的肺纤维化小鼠模型。方法 BALB/c小鼠和C57BL/6小鼠分别分成模型组和对照组,模型组气管内注射博莱霉素(5 mg/kg),对照组气管内注射相同体积生理盐水。所有小鼠于造模后第28日处死,观察肺系数、肺组织病理学改变及羟脯氨酸含量的变化。结果 光镜下各模型组肺组织呈不同程度纤维化, 其中以 C57BL/6小鼠比较为明显; 模型组的羟脯氨酸(HYP)含量均明显高于对照组; C57BL/6小鼠模型组肺系数及HYP明显高于BALB/c小鼠模型组。结论 通过气管内注射博莱霉素,BALB/c及C57BL/6小鼠均能复制肺纤维化模型,以C57BL/6小鼠肺纤维化程度比较高,获得的肺纤维化模型较为理想。肺纤维化模型的选择需要评估合适的模型来重现正在研究的纤维化形式。安徽肺纤维化模型实验外包
道喷雾博来霉素建立的特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)模型相关纤维化指标的变化。方法首先通过观察经气道给予SpragueDawley(SD)大鼠肺组织中伊文斯兰染液的分布,比较气道滴入与气道喷雾给药两种方法药物在肺组织中的分布;继而通过气道喷雾给药的方法,按5 mg/kg的剂量经气道给予实验组大鼠博来霉素,以建立IPF大鼠模型;对照组给予生理盐水。观察给药后7 d、14 d、21 d及28 d后肺组织苏木精—伊红染色(hematoxylineosin staining,HE)染色安徽肺纤维化模型实验外包炎症细胞的浸润是肺纤维化模型中的一个关键步骤。
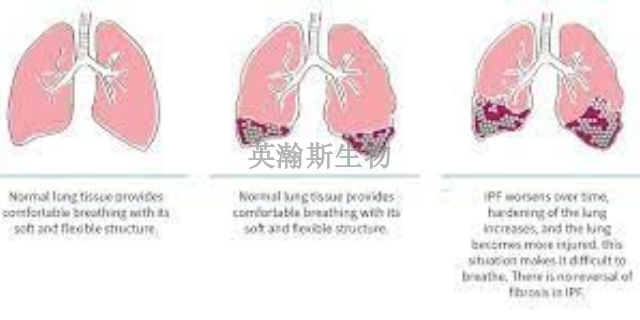
肺纤维化模型发展时间:给药后第 7 天肺组织大多呈重度肺泡炎改变,肺泡腔及肺间质内有大量中性粒细胞浸润,部分肺泡腔破坏或消失,肺间隔内成纤维细胞和***增生,与正常肺组织对比差别明显;给药后第14天,肺纤维化开始形成。巨噬细胞、中性粒细胞等炎性细胞明显减少,成纤维细胞增多,肺泡间隔明显增厚,有胶原沉积。给药后第28天,多数小鼠发生弥漫性肺间质纤维化,肺间质被胶原纤维和成纤维细胞替代,肺泡壁破坏,肺大泡形成,但仍可见炎性细胞浸润。
肺纤维化模型不仅模拟了肺纤维化的病理过程,更深入地揭示了疾病发展过程中细胞间相互作用的变化。在这个模型中,多种细胞类型如上皮细胞、成纤维细胞、免疫细胞等共同参与,并形成了复杂的细胞网络。随着疾病的进展,这些细胞间的相互作用会发生明显变化。例如,上皮细胞受损后可能释放炎症介质,刺激成纤维细胞增殖并产生过多的胶原蛋白,形成纤维组织。同时,免疫细胞的激发和迁移也会影响炎症反应的强度和持续时间。这些细胞间相互作用的变化不仅推动了肺纤维化的进展,也影响了疾病的临床表现和疗愈效果。因此,通过肺纤维化模型,研究人员可以更普遍地了解细胞间相互作用的机制,为疾病的疗愈提供新的思路和方法。肺纤维化模型揭示了疾病过程中氧化应激的作用。
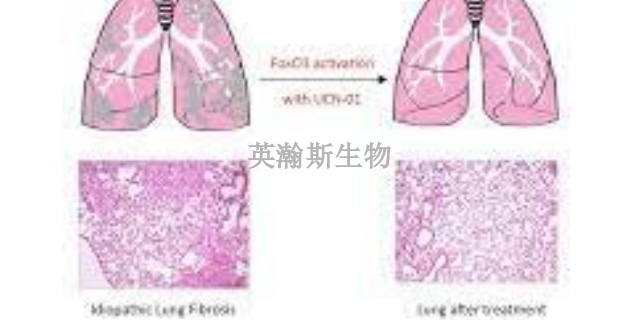
肺纤维化模型为科学家们提供了一个独特的工具,使他们能够普遍而准确地评估不同疗愈肺纤维化的方法在长期内的效果。在模型中,科学家们可以模拟疾病的自然病程和进展,从而观察并记录疗愈方法在疾病发展的不同阶段所产生的影响。这种长期模拟的能力使得科学家们能够更真实地评估疗愈方法的持久性、稳定性和安全性。通过肺纤维化模型,科学家们可以对比不同疗愈方法的长期效果,筛选出那些能够明显延缓疾病进程、改善肺功能并减少并发症的疗愈方案。这不仅为临床提供了更可靠的疗愈选择,也为患者带来了更大的希望。肺纤维化模型为研究肺纤维化与心血管疾病的关系提供了线索。安徽肺纤维化模型实验外包
科学家通过肺纤维化模型发现了一些与疾病相关的微小RNA。安徽肺纤维化模型实验外包
肺纤维化模型在肺纤维化疾病研究中扮演着重要角色,尤其是为研究疾病过程中的细胞凋亡和自噬提供了理想的实验平台。细胞凋亡和自噬是两种重要的细胞自我调控机制,它们在维持细胞稳态和应对外界压力中起着关键作用。在肺纤维化的过程中,这两种机制可能会受到干扰,导致细胞死亡和细胞功能的异常。通过肺纤维化模型,研究人员能够模拟出与肺纤维化相似的病理环境,观察和分析细胞凋亡和自噬的变化。这不仅有助于我们更深入地理解肺纤维化的发病机制,还能为开发新的疗愈策略提供科学依据。因此,肺纤维化模型为研究疾病过程中的细胞凋亡和自噬提供了宝贵的平台。安徽肺纤维化模型实验外包